Cancer du cerveau : l’Agence américaine des médicaments (FDA) booste le traitement d’ERC Belgium

Journaliste – Rédacteur en chef.
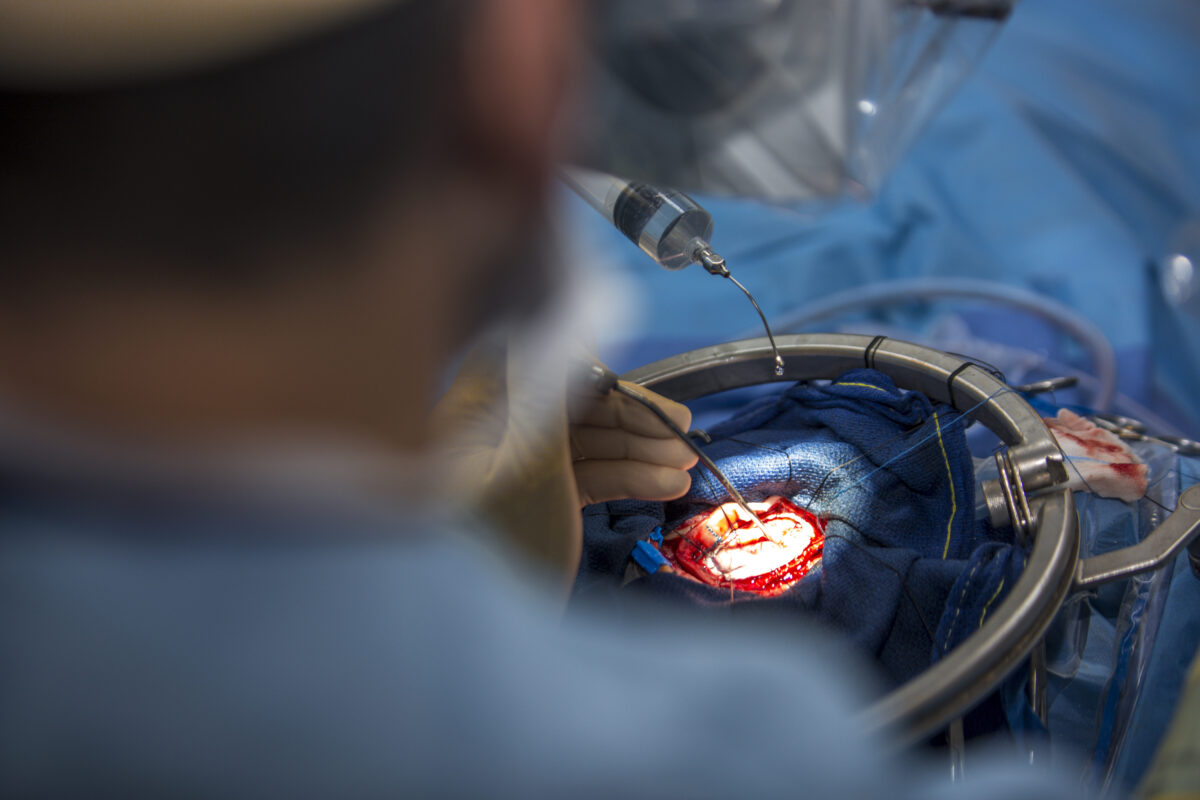 Le vaccin du Dr Stathopoulos permet de prolonger de plusieurs mois la vie des patients atteints du cancer agressif du cerveau (Glioblastome). BELGA
Le vaccin du Dr Stathopoulos permet de prolonger de plusieurs mois la vie des patients atteints du cancer agressif du cerveau (Glioblastome). BELGA L’Agence américaine des médicaments (FDA) octroie au vaccin de la société biopharmaceutique wallonne, ERC Belgium, un traitement accéléré (Fast Track) pour faciliter sa mise sur le marché. Si tout va bien, d’ici 2 ans et demi, le Gliovac ou Sitoiganap sera commercialisé, d’abord aux USA, puis en Europe, pour soulager et prolonger l’espérance de vie des patients atteints du glioblastome récurrent, la forme la plus agressive et mortelle du cancer du cerveau. ERC Belgium avait introduit une demande de commercialisation auprès de l’Agence européenne des médicaments (EMA), mais a arrêté le processus au regard de sa lenteur et de sa longueur. Mais la rapidité du processus aux USA profitera aux patients européens. ERC dit avoir les moyens financiers nécessaires pour mener à bien les tests cliniques grâce à une augmentation de capital ou encore à des engagements de soutien financier.
Bonne nouvelle pour le Dr Apostolos Stathopoulos et sa biotech wallonne, ERC Belgium, basée à Isnes (Namur). L’Agence américaine des médicaments (FDA) vient de designer la société pour bénéficier du processus Fast Track pour son traitement Sitoiganap ou Gliovac aux USA. Le Fast Track vise à faciliter la mise au point et à accélérer l’examen de nouveaux médicaments et vaccins destinés à traiter ou à prévenir des affections graves et à répondre aux besoins médicaux non satisfaits. L’objectif est de rendre de nouveaux médicaments importants accessibles plus rapidement aux patients. « Par sa décision d’accorder le Fast Track au Gliovac, la FDA reconnaît la valeur de notre traitement. Ça veut dire qu’elle reconnaît que notre traitement est supérieur à tous les traitements existants et qu’il faut lui permettre d’aller plus vite sur le marché pour sa commercialisation », se réjouit le Pr Apostolos Stathopoulos, président-fondateur et CEO d’ERC Belgium.
Futur vaccin disponible d’ici 2 ans et demi
Une réunion doit réunir, endéans le mois, les responsables de la PME wallonne et les experts de la FDA pour fixer différents objectifs (combien de patients à traiter, nouveaux protocoles, etc.), ce qui permettra à la biotech wallonne d’aller plus vite dans son processus. Son fondateur espère une mise sur le marché, d’ici deux ans et demi, du futur vaccin pour le traitement du glioblastome récurrent, la forme la plus agressive et mortelle du cancer du cerveau. Car le Fast Track garantit en fait au traitement d’ERC d’être éligible au processus d’approbation accéléré et à l’examen prioritaire de la FDA. Actuellement, le vaccin est déjà en production dans une unité aux Pays-Bas, mais uniquement à des fins de tests cliniques. Le Sitoiganap (Gliovac ou ERC1671) est une immunothérapie cellulaire du glioblastome récurrent et permet d’allonger l’espérance de vie des patients.
Il y a un an, la FDA avait déjà pris une décision peu courante d’arrêter prématurément les essais clinique de phase 2 en cours pour le Gliovac pour lui permettre d’accéder à une phase supérieure. La décision de lui faire maintenant profiter du Fast Track vient confirmer la qualité des travaux du Dr Stathopoulos et de ses équipes.
Processus trop long en Europe
La rapidité du processus tranche avec les démarches en Europe. Le Dr Stathopoulos avait introduit une demande de commercialisation auprès de l’Agence européenne des médicaments (EMA), mais il a récemment arrêté le processus. « Nous l’avons arrêté en mai, parce que ça traînait trop. Ça faisait 6 ans qu’on sollicite l’EMA, mais sans succès. On se focalise dorénavant sur les USA. De toutes façons, les patients européens pourront en profiter, car ils pourront commander le traitement dès qu’il sera mis sur le marché aux USA en attendant sa commercialisation en Europe », dit-il.
Actuellement, ERC ne commercialise pas encore de produit, mais son président-fondateur assure que la société dispose des moyens financiers nécessaires pour poursuivre ses activités. Elle aurait réalisé une nouvelle augmentation de capital ou dispose d’engagement de partenaires pour la soutenir financièrement. Elle occupe une vingtaine de collaborateurs et a des filiales à l’étranger (USA, Pays-Bas, Canada, Australie). Elle est aussi présente dans d’autres contrées à l’international grâce à des accords spécifiques à chaque pays en Europe et en Amérique latine.


